09.30
【10月1日より接種開始】新型コロナ「レプリコン・ワクチン」は本当に大丈夫なのか?ワクチンの第一人者が答える 「5人死亡」「18人死亡」「エクソソーム」「日本だけ承認」……ネットなどの指摘をどう読むか(1/6) | JBpress (ジェイビープレス)
石井氏は、レプリコン・ワクチンに関する懸念が挙がっていることについて、次のように述べた。「メディアでワクチンに対する不安を煽る記事が増えている現状ですが、私の研究や論文を基にした見(1/6)
この9月、厚生労働省が、自己増殖型mRNAワクチン、いわゆる「レプリコン・ワクチン」を承認した。10月から接種開始となる。
レプリコン・ワクチンを巡っては、名前の通り自己増殖型という新しい仕組みを持つこともあり、接種した後にワクチンの成分がいつまでも増え続けて、体内に想定外の悪影響をおよぼすのではないかという懸念が広がっている。
しかも、海外の他国ではまだ承認されておらず、日本で初めて実用化されることもあって、不安の声が助長されているところもある。一般の人ばかりではなく、医療関係者からも不安の声がある。
一方で、ネット上にある情報は、断片的なものが多く、引用文献の扱いも不十分なものも目立つ。本当にその心配は的を射ているのだろうか。
獣医師資格を持ち、医療分野のジャーナリストとして25年近くになる筆者としては、もう少し確度の高い情報を提示すべきだと感じている。
そこで、今回は原典に当たった上で、レプリコン・ワクチンの承認プロセスなどについて中立の立場にあるワクチン研究の第一人者、東京大学医科学研究所ワクチン科学分野教授の石井健氏にも取材し、レプリコン・ワクチンを巡る不安に答えていく。(星良孝:ステラ・メディックス代表/獣医師/ジャーナリスト)
検証する上で当たるべき2つの原典
石井氏は、レプリコン・ワクチンに関する懸念が挙がっていることについて、次のように述べた。
「メディアでワクチンに対する不安を煽る記事が増えている現状ですが、私の研究や論文を基にした見解をお話しすると、現時点ではワクチンに重大な問題があるとは考えていません。ただし、新しい技術に対する不安は当然のことで、そのような懸念が出ることについては理解しています」
コロナ禍で多くの人が不安を感じたと思うが、ワクチンを巡ってはさまざまな議論が出る傾向にある。レプリコン・ワクチンについても多くの意見が出ているが、ネット上にある懸念の中で重大だとされているのが、レプリコン・ワクチンを接種すると死亡のリスクが高まるという指摘だ。これについてまずは検証する。
この懸念については、大きく2つの原典に当たることでどういうことかを理解することができる。
・レプリコン・ワクチンの安全性と有効性を確かめた臨床試験の論文
・レプリコン・ワクチンの日本での承認審査に使われた承認審査報告書
最初に臨床試験を検証しよう。
「臨床試験で5人が死亡」の言説はどう解釈すべきか?
2024年に発表された臨床試験の論文は、第1相~第3相までの試験情報をまとめて報告したものだ。医薬品は、第1相~第3相と段階を踏んで、人数を増やしながら、慎重にその安全性や有効性を確認している。
ネット上で問題とされたのは第3b相という最終段階の試験で死亡者が出ており、これがワクチンと関連するという疑念が持たれていることだ。
この試験を見てみると、対象者は約1万6000人とかなり多いことが分かる。試験では、対象者が2つのグループに分けられ、片方の約8000人にはレプリコン・ワクチン、もう片方の約8000人にはプラセボ(偽薬)が接種された。
試験の期間は92日間が設定され、この間に両方のグループを合わせて合計21件の死亡が報告された。この死亡について懸念が集まっているわけだが、内訳としては、レプリコン・ワクチンの接種を受けた群では5人、プラセボの群では16人が死亡した。
一部のネットの情報では、ワクチン接種を受けた群で5人が死亡したことが問題視されているが、プラセボ群の16人と比べると割合は少ない。
「21人死亡」という話も出ているが、それはレプリコン・ワクチン群とプラセボ群を合わせた死亡数が21人のため。ただ、プラセボ群の死亡はそもそもワクチンと関連しない。
論文によると、死亡者のうち、ワクチン接種に関連した死亡は一件も確認されず、コロナ感染に関連する死亡が10件(ワクチン接種者1人、プラセボ接種者9人)報告された。これもワクチン接種の群の方が少ない結果となっている。
そのほかの死亡は、がんによる死亡などで、ワクチンでこれまで問題になった心臓や血管に関わるものは、プラセボ群の大動脈解離に限られた。
※1~92日目における死亡例は、レプリコン・ワクチン群5/8059 例(0.1%、低血糖、膵炎、肺の悪性新生物、咽頭癌転移、コロナ感染が各1例)、プラセボ群16/8041例(0.2%、コロナ感染が9例、リンパ節腫脹、肝硬変、肝がん、大動脈解離、肺炎、アシネトバクター性肺炎、敗血症性ショックが各1例)
8000人もの大勢が試験に参加すると統計的に死亡者が出ることもある。他の医薬品の臨床試験でも珍しくはない。
ネットの言説では、5人が亡くなったという点が強調されているものも見られるが、全体の人数と死亡の割合を見ると、冷静に医薬品の安全性を評価することができる。
後述するが、レプリコン・ワクチンは新しいものなので、今後の不確定要素はあるのだが、この臨床試験に限ってみれば、ことさら強調するのは妥当とは言えないのではないか。
石井氏もこの臨床試験については「第1相から第3相までの臨床試験を経て、安全性と有効性は十分に確認できている」と解釈する。新しい技術を用いたワクチンの不確定要素については石井氏も慎重に見守るべきだというが、それについては後述する。
「18人が死亡」という懸念の声をどう考える?
続いて、日本での承認審査に使われた承認審査報告書についても見る。
ネットの指摘では、この審査報告書の追加データにおいても死亡が報告されていると問題視されている。例えば、ネットでは「18人が死亡した」と批判する意見が確認できる。
これはどういうことだろうか。
報告書では、臨床試験の論文に掲載された92日目よりも後の210日目までの情報が掲載されている。92日目よりも後はレプリコン・ワクチンとプラセボの入れ替えが行われ、その影響が評価されている。
具体的には、92日目までにレプリコン・ワクチンの接種を受けていた人は一転、プラセボの接種を受け、逆にプラセボの接種を受けていた人はレプリコン・ワクチンの接種を受けるという入れ替えが行われた。医薬品の効果が一方のグループに偏らないように入れ替えが行われるのは、医薬品の試験ではよく行われることだ。
こうして2つのグループが観察された結果、レプリコン・ワクチン―プラセボの順番で接種を受けたグループでは9人が、プラセボ―レプリコン・ワクチンの順番で接種を受けたグループでは4人が死亡した。
ネット上では、92日以降に両方の群を合わせて合計13人が亡くなったのではないかという指摘が見られる。92日目までにレプリコン・ワクチンの接種を受けた群で亡くなった5人も加えて、合計18人が亡くなったというものだ。
こちらについても、両方の群が約7500人存在し、それらの中で4カ月ほどの期間で亡くなった人は全体の0.1%に過ぎない。心筋梗塞や脳血管発作といった心血管関連の死因があったが、1万5000人中2人であり、その頻度は極めて低い。ワクチンが原因と断定するのは無理があるように見える。
石井氏は審査報告書の死亡については、「これらがワクチンが原因になったと懸念することは論理に飛躍があるのではないかと考えます」と説明する。
※レプリコン・ワクチン―プラセボ群9/7458例(0.1%、事故死、他の特定できない死亡が各2例、急性心筋梗塞、敗血症性ショック、外傷、口唇がん/口腔がん、悪性肺新生物が各1例)、プラセボ―レプリコン・ワクチン群4/7349例(0.1%、コロナ感染が2例、頭蓋脳損傷、脳血管発作が各1例)
自己増殖リスクは高いか、低いか?
レプリコン・ワクチンに関する代表的な懸念として自己増殖するというメカニズムに対するものもある。
審査報告書に書いてあるが、レプリコン・ワクチンは、ベネズエラ馬脳炎ウイルスというウイルスの持つ、「レプリカーゼ」というRNAを増殖させる機能を持つタンパク質と、これまでのコロナワクチンでも使用されたコロナのSタンパク質という2種類のタンパク質をコードするmRNAをワクチンにしたものだ。
自己増殖の機能を持つタンパク質はウマ由来のウイルスを使用しているため、安全性が担保されていると考えられる。異なる種のウイルスは感染性が異なり、無害となることが多い。
その上で、自己増殖するというレプリコン・ワクチンのメカニズムは安全であるのかという点が懸念材料になっている。
「レプリコン・ワクチンに対する懸念は、このワクチンが新しい仕組みを持つからですが、臨床試験や実際の使用データから見ると、現在までのところ自己増殖リスクは非常に低いと考えられます」と石井氏は評価する。
その上で、石井氏は、レプリコン・ワクチンは、ウイルスを使ったワクチンと、mRNAワクチンの中間であると指摘する。
従来のワクチンの中には、ウイルスそのものが使われ、体内で増殖する性質を持つものもある。一方、mRNAを使用したワクチンとしては従来のコロナワクチンがあり、これは世界中で使用実績がある。レプリコン・ワクチンはこれら双方の特徴の一部を併せ持っていると考えられるというのだ。
「『レプリコン・ワクチンが自己増殖する』という不安や懸念については理解できますが、自己増殖する性質は通常のウイルスを使ったワクチンでも確認されていることです。例えば、風疹、麻疹、黄熱などのワクチンは、ウイルスそのものを使っており、体内で増殖します。それらは副反応のリスクがあります」
確かに、既に普及しているワクチンの中には、ウイルス自体を使っているものは珍しくない。麻疹、いわゆるはしかのワクチンは、幼少期の接種が一般化している。体内で増殖するワクチンだが、懸念なく接種が広がっているのは、実績が多いからだろう。
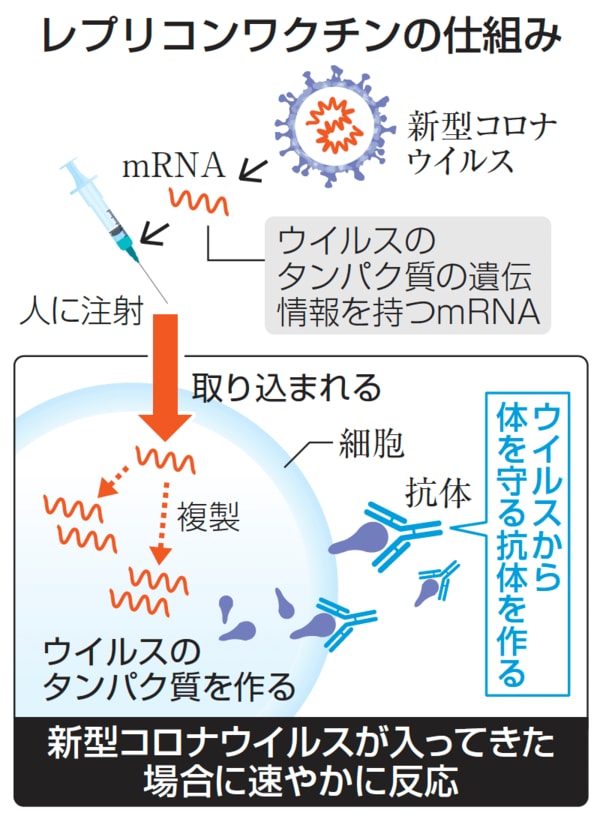 レプリコン・ワクチンの仕組み(図表:共同通信社)
レプリコン・ワクチンの仕組み(図表:共同通信社)拡大画像表示
「安全性」と「安心」の違いをどう考える?
石井氏が強調するのは次の点だ。
「ここで重要なのは『安全性』と『安心』の違いです。安全性は科学的に確認されたものですが、安心感はそれに基づく心理的なものです。例えば、mRNAワクチンが最初に登場した際には、その安全性に対する不安が広がりましたが、リアルワールドデータ(実際に広く使われたデータ)が蓄積されるにつれて、徐々に安心感が高まりました。この安心感が完全に得られるまでには時間がかかります」
つまり、臨床試験などから「安全性」が確認されても、その後、実際の使用過程でデータが蓄積されることで、「安心」が得られる。
「治験で確認された安全性や有効性は非常に重要ですが、ワクチンが広く使用されることによってリアルワールドデータが蓄積され、さらなる検証が行われます。例えば、mRNAワクチンで確認されたアナフィラキシーや心筋炎のような副作用は、治験段階では十分に検出されないことがあります。これらは実験的に検討するのは難しいことが分かっています。実際に多くの人々が接種することで、これらのまれな副作用が明らかになってくるわけです」(石井氏)
逆に言えば、副反応が問題視されることで、そのワクチンは普及しないという結果も当然ある。
石井氏は、「実際、コロナワクチンの中でも、アストラゼネカやジョンソン・エンド・ジョンソンののワクチンはアデノウイルスというウイルスを使用しましたが、血栓症のリスクが市販後の調査で確認されました。結果として、普及しませんでした」と解説する。
今後、レプリコン・ワクチンが、これまで観察されていない副反応を伴うことがあれば、そもそも普及していかない可能性もある。
「シェディング」や「エクソソーム」など、自己増殖したワクチンが体外に排出されるという指摘もネットなどの意見では目にすることがある。
石井教授は、「シェディングやエクソソームに関する懸念は、従来のウイルスベクターワクチンでも同様でしたが、理論的には理解できるものの、現実にはリスクが非常に低いです。これらの懸念を科学的に証明するためには動物モデルが必要ですが、低頻度で起こり得る事象で、動物モデルでの検証は困難です」と述べる。
こうした面での安全性を確かめるためにも、リアルワールドデータは重要になる。確かに懸念はあるが、ごくまれに起こるものを過剰に重く見て、有望な技術を反故にするのは賢明とは言えない。
「実際に広く使用された後のデータにより、懸念が科学的に検証され、データが蓄積されることで、最終的には不安を解消していくのが重要と考えています」(石井氏)
リスクを理解し、ベネフィットとのバランスで考える
ワクチンの安全性や有効性の審査は、臨床試験によって検証され、統計学的に安全なのか、有効なのかが慎重に確かめられることになる。
先述したように、客観的にデータを検証すると、今回の臨床試験や審査報告書に基づけば、210日目までの安全性は確認されたといえるのではないかと、筆者は考える。過度に不安視すべき内容ではない。
もちろん、死亡が出ていることなど、健康への悪影響の可能性は完全には否定できない。ワクチンと健康への影響の因果関係については、引き続きワクチン接種を受けた人たちを慎重に観察しながら安全性を評価していく姿勢も重要だろう。
審査報告書までのデータでは、安全性と有効性が確認されたとはいえ、参照できるのは210日目までのデータに限られる。これから先の情報は不足しており、未確認のリスクが存在することは事実だ。その上で、利用するかどうかをベネフィットを考えながら、判断することになる。
未確定のリスクがあるのは事実であり、慎重に自ら必要とするかを判断することは理にかなっている。
「リスクベネフィットの観点からいうと、コロナウイルスで重症化するリスクの高い人にとっては、一般的にワクチンのベネフィットが大きいと考えられます。レプリコン・ワクチンについても、リスクの高い人にとってはベネフィットが高くなりますから、未確認のリスクの可能性を踏まえても、接種の有用性はあるといえるでしょう。一方、感染による重症化リスクが低い小児や健康な成人などでは、ベネフィットが不明確な点があるため、未確認のリスクを踏まえて、推奨されないという判断になります」と石井氏は説明する。
10月1日から始まる定期接種において、レプリコン・ワクチンの対象者は65歳以上の高齢者と、60歳から64歳のリスクの高い人とされている。対象者は公費による助成がある。一方で、それ以外の人たちは任意接種となり、公費による助成はなく自費負担となる。
また、日本でのみ承認された点について、他国で未承認であることが懸念される場合もある。
石井氏は、「逆に、日本で承認されていない医薬品が、米国や他の国々で先に承認されている例はよくあります。これは各国の規制当局の判断基準やプロセスの違いに基づくもので、日本で承認されていないからといって、その医薬品やワクチンが危険だと決めつけるのは論理の飛躍でしょう」と述べる。
各国で承認申請が進められている中、日本のみで承認された背景には、最近の日本における医薬品承認プロセスの高速化が関係していると思われる。
かつて、ドラッグラグと呼ばれ、日本では医薬品の承認が長期間遅れていたことが問題視されていた。漫画「ブラックジャックによろしく」ではドラッグラグが苦々しいものとして描かれていると思うが、今回のワクチン承認が早すぎるという問題は隔世の感がある。
前提として、原典情報のある客観的なデータを踏まえて判断する必要がある。その上で、未確認のリスクについて理解しながら、接種を受ける本人の健康リスクを踏まえて、ベネフィットを判断し、是々非々で接種の必要性を判断することが重要である。
【参考文献】
◎Hồ, N.T., Hughes, S.G., Ta, V.T. et al. Safety, immunogenicity and efficacy of the self-amplifying mRNA ARCT-154 COVID-19 vaccine: pooled phase 1, 2, 3a and 3b randomized, controlled trials. Nat Commun 15, 4081 (2024). https://doi.org/10.1038/s41467-024-47905-1
◎審議結果報告書
星 良孝(ほし・よしたか)
ステラ・メディックス代表取締役/編集者 獣医師
東京大学農学部獣医学課程を卒業後、日本経済新聞社グループの日経BPにおいて「日経メディカル」「日経バイオテク」「日経ビジネス」の編集者、記者を務めた後、医療ポータルサイト最大手のエムスリーなどを経て、2017年に会社設立。獣医師。
ステラ・メディックス:専門分野特化型のコンテンツ創出を事業として、医療や健康、食品、美容、アニマルヘルスの領域の執筆・編集・審査監修をサポートしている。また、医療情報に関するエビデンスをまとめたSTELLANEWS.LIFEも運営している。
・@yoshitakahoshi
・ステラチャンネル(YouTube)
コメント
この記事へのトラックバックはありません。




この記事へのコメントはありません。